智科医疗有专业团队依据《医疗器械生产监督管理办法》(国家食品药品监督管理总局令第 7 号)、《医疗器械生产质量管理规范》、《医疗器械生产质量管理规范附录体外诊断试剂》及《医疗器械生产质量管理规范体外诊断试剂现场检查指导原则》,并结合产品实际情况建立质量管理体系,形成质量手册、程序文件、支持性文件及质量记录,实施、保持和改进质量管理体系的有效性。同时,对质量管理体系的适宜性、充分性进行一站式法规技术辅导,帮助企业建立健全与所生产医疗器械相适应的质量管理体系,确保产品质量在采购、生产、形成和实现的全过程都能得到有效控制。
质量管理体系文件包括:
1)质量方针、质量目标;
2)质量手册;
3)ISO13485:2016、《医疗器械生产监督管理办法》的要求,根据公司质量管理体系需要所形成的程序和文件,包括技术文件、管理文件与外来文件;
4)《医疗器械生产质量管理规范》要求的记录;
5)国家或地区法规规定的其它文件等;
6)文件的形式:纸质文件。
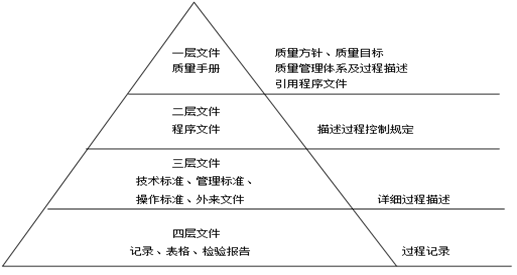
质量管理体系的文件结构: